Рандомизированные контролируемые исследования являются золотым стандартом получения научных данных о новых медицинских вмешательствах. Это означает, что выпуская новый лекарственный препарат на рынок, фармацевтическая компания обязана проверить как эффективность, так и безопасность своего препарата, проведя рандомизированное контролируемое исследование (РКИ).
Рандомизированное контролируемое исследование в медицине

Читая статьи, и получая консультации на нашем сайте, вы част.
Это означает, что выпуская новый лекарственный препарат, новый метод диагностики или лечения, компания-производитель должна проверить как эффективность, так и безопасность своего метода исследования или лечения, проведя рандомизированное контролируемое исследование (РКИ).
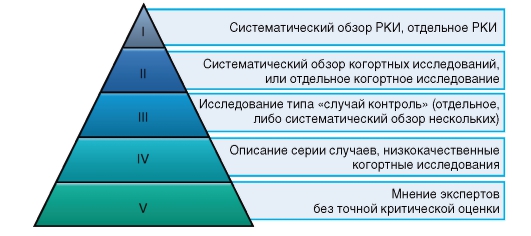
На схеме показана т.н. пирамида доказательности. Как видите РКИ занимает первое место в этой иерархической системе.
Что же означают эти три слова в данном методе клинического анализа: рандомизированное контролируемое исследование?
Рандомизированное – означает, что решение о том, в какую группу попадет пациент, в испытательную (ту, в которой будут испытывать новый метод), традиционную (ту, в которой будет использоваться общепринятое лечение данного заболевания) или в контрольную (ту, в которой будут использовать плацебо, то есть «пустышку») принимается совершенно randomly.
Контролируемое – означает, что в исследовании обязательно будет осуществляться контроль, путем сравнения с традиционным методом лечения, или с группой плацебо.
Study – напоминает, что препарат проходит испытание, в ходе которого он обязан показать как свою эффективность в лечении этой патологии, так и свою безопасность, в противном случае ему никогда не попасть в аптеки.
Почему в клинических исследованиях требуется рандомизация?
Random отбор кандидатов крайне важен, поскольку в противном случае, если мы предоставим пациенту или врачу выбирать, в какую группу поместить участника исследования, это может сильно исказить полученные результаты.
Thanks to рандомизации мы избавляемся от всякой предвзятости и делаем группы максимально однородными: по полу, возрасту, анамнезу, длительности заболевания, осложнениям, сопутствующим заболеваниям и т.д., чтобы сократить количество искажений результатов исследования от посторонних факторов до минимума.
Скажем, если врач очень хочет получить положительные результаты от изобретенного им препарата, он может сознательно или неосознанно помещать более тяжелых пациентов в группу плацебо (т.е. в группу контроля), а менее тяжелых пациентов – в группу, получающую экспериментальный препарат. Тогда он гарантированно получит в экспериментальной группе лучшие показатели лечения, но таким показателям совсем нельзя будет доверять.
And now imagine that the doctor would not just like to get good results, but also bribed the pharmaceutical company directly interested in the most positive results of the study of their new drug. In this case, the rates are very high, and financial flows are also. That is why, by conducting careful randomization of patients, we exclude not only any bias, but any random distortion.
Why are clinical trials "controlled"?
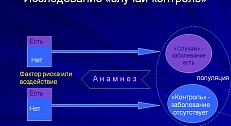
Study Case-Control
Investigation of the "case-control" type is one.
"After that – does not mean due to" – They said more ancient Romans. If you do not compare with the control groups, you can get a pronounced positive or pronounced negative effect that has nothing to do with the studied drug, and mistakenly establish yourself in thought that there is a direct causal connection between the drug and this effect.
Another mandatory property of a study that increases the degree of control is the presence of a sufficiently large number of research participants. It is necessary that random differences and unusual cases do not have a big impact on the results obtained.
The control group usually gets Placebo: This is a dummy, which looks like, has the taste of an identical real drug, but does not contain a valid substance.
Comparison with standard treatment
In addition to the placebo group, the comparison often occurs with the group obtained by the standard and generally accepted with the studied pathology, treatment. The purpose of such a comparison is to determine what the advantages and what are the risks of experimental therapy compared with the standard one.
The fact that the new drug has a therapeutic effect with a given disease is insufficient for approval and widespread use. It should be more efficient and / or more safe than standard generally accepted therapy, at least in some cases under certain known conditions.
In addition to all this, it is important is the cost of new therapy, in comparison with the cost of standard treatment. If the drug is less efficient, but much cheerful is to become an argument in its favor.
Impracticality and placebo inethealth in some RKK
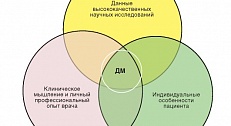
Evaluation of the quality of medical information
Not all medical studies provide equally hope.
- Many aggressive or invasive procedures (using a special medical apparatus, or using a surgical operation), or unethical imitate. It is impossible to cut a fabric to a man, only that he does not guesses where it is in the medical, or in control groups.
- The disease can be too rare, and scientists have no opportunity to dial such a number of patients that will ensure the accuracy of the scientific data obtained.
- Matching patients to a particular study can be too difficult.
If such obstacles do not allow RCTs, then a different, more appropriate design is chosen for such a study. The decision on the admissibility of RCTs is made by a special ethics committee. A clinical trial cannot be started without the approval of this committee.
